31 ตุลาคม 2565 คณะวิทยาศาสตร์ มหาวิทยาลัยมหิดล จัดเสวนาพิเศษ Nobel Prize in Mahidol Science Cafe Vol.2: สู่ยุคของโมเลกุลเชิงหน้าที่ Click Chemistry and Bioorthogonal Chemistry: Entering the Era of Functionalism แบบ Hybrid ซึ่งนับเป็นตอนที่ 2 ของเสวนาซีรีส์โนเบลประจำปี 2565 โดยได้รับเกียรติจากอาจารย์ผู้เชี่ยวชาญการสร้างและประยุกต์ใช้ Click Chemistry and Bioorthogonal Chemistry ของมหาวิทยาลัยมหิดล อาทิ รองศาสตราจารย์ ดร.ปรียานุช แสงไตรรัตน์นุกูล อาจารย์ประจำภาควิชาเคมี คณะวิทยาศาสตร์ อาจารย์ ดร.สิทธิวุฒิ เจริญสุทธิวรากุล อาจารย์ประจำกลุ่มสาขาวิชาชีวนวัตกรรมและผลิตภัณฑ์ฐานชีวภาพอัจฉริยะ คณะวิทยาศาสตร์ อาจารย์ ดร.ณัฐวดี ปัญญาอินทร์ อาจารย์ประจำภาควิชาชีวเคมี คณะวิทยาศาสตร์ และ อาจารย์ ดร.มัทธิว พันชนะ อาจารย์ประจำ ภาควิชาชีวโมเลกุลและพันธุศาสตร์โรคเขตร้อน คณะเวชศาสตร์เขตร้อน ร่วมพูดคุยเจาะลึกเกี่ยวกับเรื่องราว การวิจัย และสาระน่ารู้ของการพัฒนาคุณสมบัติโมเลกุลและเซลล์ด้วยปฏิกิริยาคลิก ซึ่งเป็นการเปิดประตูสู่ยุคของการศึกษาและสร้างสรรค์โมเลกุลเชิงหน้าที่ ณ ห้อง K102 อาคารเฉลิมพระเกียรติ คณะวิทยาศาสตร์ มหาวิทยาลัยมหิดล พญาไท และถ่ายทอดสดผ่านทาง Facebook live โดยมีผู้รับชมรวมกว่า 50 คน
รองศาสตราจารย์ ดร.ปรียานุช แสงไตรรัตน์นุกูล ได้กล่าวถึงผู้ได้รับรางวัลโนเบล สาขาเคมี ในปี ค.ศ. 2022 นี้ ได้แก่ ศาสตราจารย์ มอร์เทน เมลดัล (Morten Meldal) จากมหาวิทยาลัยโคเปนเฮเกนประเทศเดนมาร์ก ศาสตราจารย์ เค. แบร์รี ชาร์ปเลส (K. Barry Sharpless) จากสถาบันวิจัยสคริปส์ประเทศสหรัฐฯ ผู้ศึกษาเกี่ยวกับ “Click Chemistry” หรือ “ปฏิกิริยาคลิก” และ ศาสตราจารย์ คาโรลีน อาร์. เบอร์ทอซซี (Carolyn R. Bertozzi) จากมหาวิทยาลัยสแตนฟอร์ดประเทศสหรัฐฯ นักวิทยาศาสตร์หญิงผู้ต่อยอดปฏิกิริยาคลิกสู่ศาสตร์ “Bioorthogonal Chemistry” หรือ “เคมีไบโอออร์โทโกนอล” โดยในปีนี้ ศาสตราจารย์ ชาร์ปเลส เป็นบุคคลที่ 5 ตั้งแต่เริ่มมีการประกาศรางวัลโนเบล ที่ได้รับรางวัลโนเบลถึง 2 ครั้ง
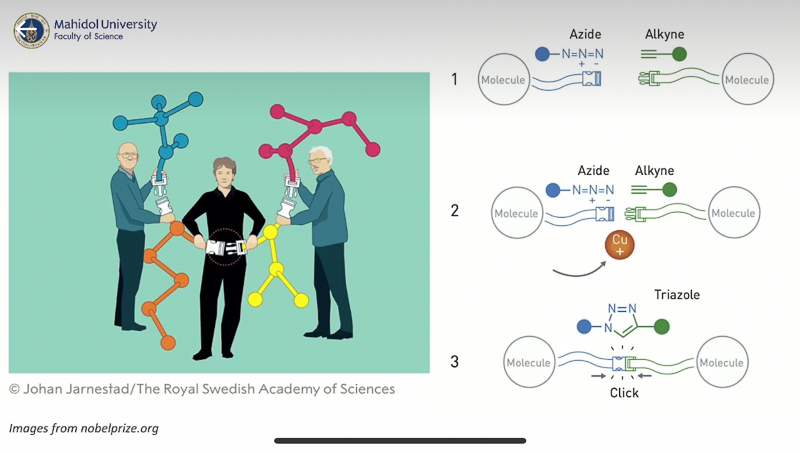
ในปี ค.ศ. 2001 Sharpless และผู้ร่วมงานได้ตีพิมพ์แนวคิดของ “ปฏิกิริยาคลิก” ว่าเป็นปฏิกิริยาที่เชื่อมต่อโมเลกุลเข้าด้วยกันอย่างเรียบง่าย รวดเร็ว และมีขอบเขตที่กว้าง โดยไม่ใช้ตัวทำละลาย หรือใช้ตัวทำละลายที่ไม่เป็นพิษ และให้ร้อยละผลิตภัณฑ์สูง ผลพลอยได้จากผลิตภัณฑ์ (by-products) ไม่เป็นพิษ สามารถกำจัดออกได้โดยไม่ต้องใช้เทคนิคในห้องปฏิบัติการทางเคมีเพื่อใช้ในการแยกสารผสม และมีแรงผลักทางพลังงานสูง เปรียบการเชื่อมต่อโมเลกุลเหมือนกับการใส่หัวเข็มขัด และเสียงคลิกคือปฏิกิริยาที่เกิดขึ้น โดยปฏิกิริยาที่เข้าข่ายปฏิกิริยาคลิก ได้แก่ Diels-Alder thiol-ene และ 1,3-dipolar cycloaddition เป็นต้น
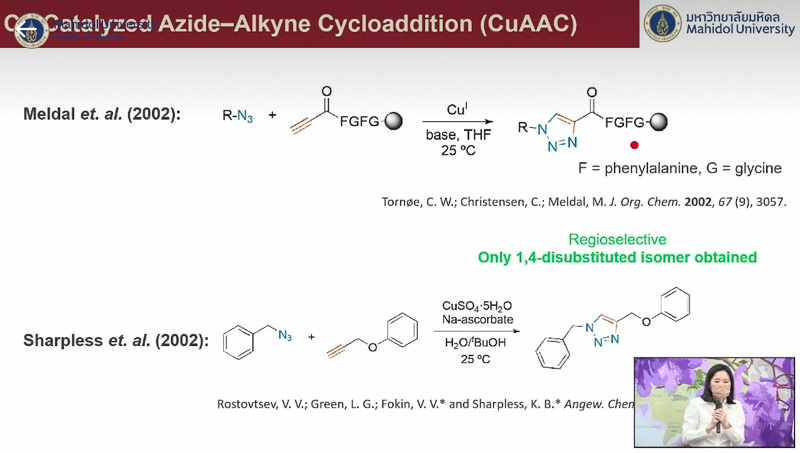
ก่อนกล่าวถึงงานวิจัยสำคัญของ เมลดัล และ ชาร์ปเลส ซึ่งได้รับตีพิมพ์ในปี ค.ศ. 2002 ในเวลาใกล้เคียงกัน ที่ศึกษาปฏิกิริยาระหว่างโมเลกุลที่มีหมู่ฟังก์ชัน “อะไซด์” (azide) กับ “อัลไคน์” (alkyne) โดยมีตัวเร่งปฏิกิริยาเป็นไอออนของทองแดง (Cu+) ซึ่งจัดเป็นปฏิกิริยาคลิก โดย เมลดัล ใช้คอปเปอร์ (I) ไอโอไดด์ เป็นตัวเร่งปฏิกิริยา ส่วน ชาร์ปเลส ใช้คอปเปอร์ (II) ซัลเฟต ซึ่งราคาถูกและเสถียรกว่า และเกลือของวิตามินซีเป็นตัวรีดิวซ์ เพื่อให้ตัวเร่งปฏิกิริยา Cu+ ในสารละลาย และได้เรียกชื่อปฏิกิริยาว่า Cu-Catalyzed Azide–Alkyne Cycloaddition หรือ CuAAC ผลการศึกษาของทั้ง 2 กลุ่มวิจัย พบว่าปฏิกิริยามีประสิทธิภาพสูง เหมาะกับการเติมหมู่ฟังก์ชันหรือสังเคราะห์วัสดุใหม่ ๆ เนื่องจากปฏิกิริยา CuAAC ได้รับความนิยมเป็นอย่างมาก เพราะหมู่ฟังก์ชัน azide และ alkyne ไม่ซับซ้อน สามารถเติมเข้าไปในโมเลกุลสารตั้งต้นได้ง่าย และตัวเร่งคอปเปอร์มีความเรียบง่าย ปฏิกิริยาเกิดได้ดี ทำให้ในปัจจุบันปฏิกิริยาคลิก มักสื่อถึงปฏิกิริยา CuAAC ถึงแม้ว่าในความเป็นจริงมีหลายปฏิกิริยาที่จัดเป็นปฏิกิริยาคลิกตามที่กล่าวไปข้างต้น
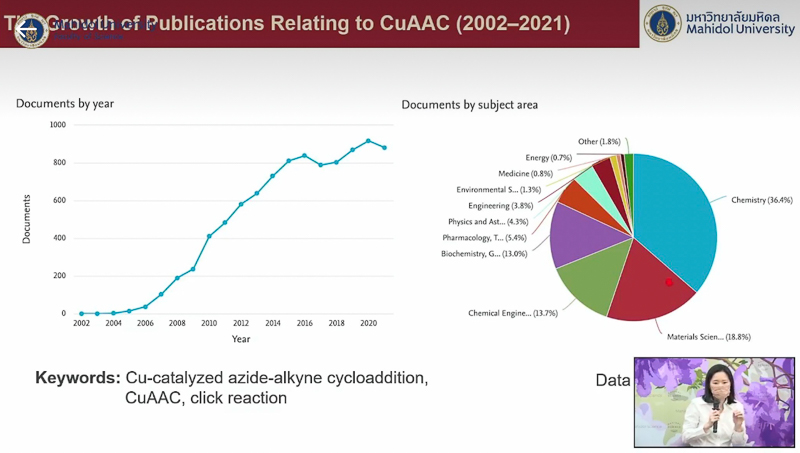
นับจากการค้นพบที่สำคัญของเมลดัลและชาร์ปเลสในปีค.ศ. 2002 จนถึงปัจจุบัน เป็นระยะเวลาประมาณ 20 ปี มีผลงานวิจัยเกี่ยวกับปฏิกิริยาคลิกตีพิมพ์เกือบ 10,000 ผลงาน และมีการนำไปใช้ในการศึกษาวิจัยหลายด้าน ทั้งด้านเคมี วิศวกรรมเคมี วัสดุศาสตร์ การสังเคราะห์ยา การแพทย์ และสิ่งแวดล้อม เป็นต้น โดยคณาจารย์ภาควิชาเคมีและนักศึกษาคณะวิทยาศาสตร์ก็ได้นำเอาแนวคิดปฏิกิริยาคลิกมาประยุกต์ใช้กับงานวิจัยด้วยเช่นกัน อาทิ การสร้างระบบเร่งปฏิกิริยาที่สามารถละลายน้ำได้ ไม่เป็นพิษต่อสิ่งแวดล้อม และสามารถนำตัวเร่งปฏิกิริยากลับมาใช้ซ้ำได้ การพัฒนาฟลูออเรสเซนต์เซนเซอร์ และเซนเซอร์เปลี่ยนสีที่มีความจำเพาะสูง เพื่อตรวจวัดไอออนของเหล็ก และคอปเปอร์ รวมถึงตรวจวัดไอออนไซยาไนด์ และคลอไรด์ในน้ำ การสังเคราะห์โมเลกุลขนาดใหญ่และศึกษาสเปซเซอร์ของโมเลกุล เพื่อเพิ่มประสิทธิภาพการตรวจจับไอออนของไอโอไดด์ และ มาโลเนต เป็นต้น นอกจากนี้ ยังกล่าวถึงงานวิจัยที่นำปฏิกิริยาคลิกมาพัฒนาระบบนำส่งยาคีโมที่มีความจำเพาะสูงต่อเซลล์มะเร็งบางประเภท การปรับปรุงคุณสมบัติพอลิเมอร์ให้สามารถเชื่อมปิดพื้นผิวบริเวณที่เสียหายเองได้และเรืองแสงแสดงตำแหน่งที่เกิดการขีดข่วน รวมถึงการนำปฏิกิริยาคลิกไปใช้เป็นขั้นตอนสำคัญในการสังเคราะห์ยาฆ่าเชื้อแบคทีเรีย และยารักษามะเร็งเต้านม เป็นต้น




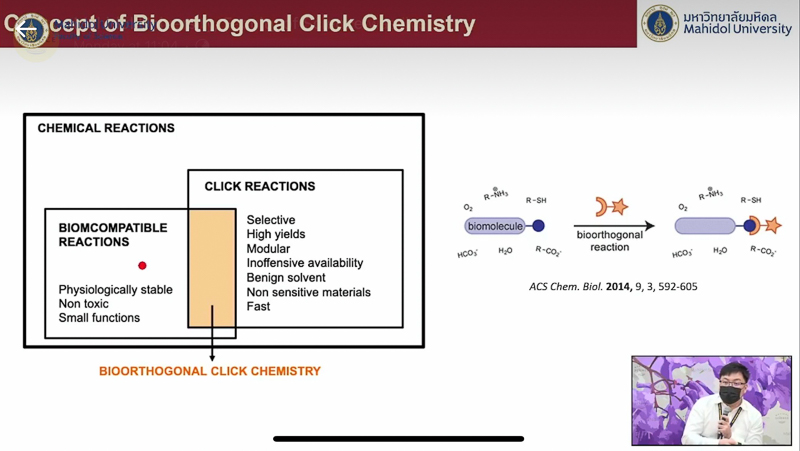
จากนั้น อาจารย์ ดร.สิทธิวุฒิ เจริญสุทธิวรากุล ได้กล่าวถึงงานวิจัยของ ศาสตราจารย์ คาโรลีน อาร์. เบอร์ทอซซี จากมหาวิทยาลัยสแตนฟอร์ดของสหรัฐฯ นักวิทยาศาสตร์หญิง อีกหนึ่งในผู้ได้รับรางวัลโนเบล สาขาเคมีในปีนี้ ที่ต่อยอด “Click Chemistry” ไปสู่ “Bioorthogonal Chemistry” โดยผสมผสานระหว่างปฏิกิริยาคลิก (Click reactions) ที่เกิดขึ้นเร็ว มีขอบเขตกว้าง ให้ผลิตภัณฑ์สูง กับปฏิกิริยาที่เข้ากันได้ทางชีวภาพ (Biocompatible reactions) ที่ไม่เป็นพิษต่อเซลล์ มีความเสถียร มีฟังก์ชันขนาดเล็ก เกิดเป็นแนวคิดของปฏิกิริยาที่สามารถทำให้เกิดขึ้นในระบบสิ่งมีชีวิตได้โดยไม่มีการแทรกแซงจากสิ่งแวดล้อมรอบข้าง
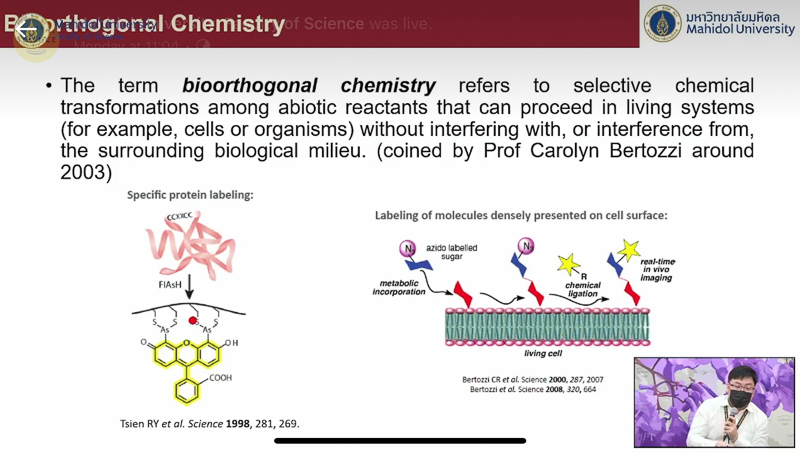
หนึ่งในปฏิกิริยาแรก ๆ ที่จัดได้ว่าเข้าข่ายเป็น “เคมีไบโอออร์โทโกนอล” คืองานวิจัยในปี ค.ศ. 1998 ของโรเจอร์ เฉียน (Roger Y. Tsien) เจ้าของรางวัลโนเบล สาขาเคมี ปี ค.ศ. 2008 ซึ่งทำการติดฉลากสีบนโปรตีน ทำให้สามารถรายงานได้ว่าโปรตีนที่เราสนใจอยู่ตรงไหน และงานวิจัยของศาสตราจารย์เบอร์ทอซซี ในปี ค.ศ. 2000 ที่นำเอาโมเลกุลของน้ำตาลที่มีหมู่ฟังก์ชันอะไซด์ ติดลงบนผิวเซลล์ และนำมาคลิกกับอัลไคน์ที่ผิวเซลล์ ทำให้สามารถรายงานได้ว่าน้ำตาลดังกล่าวอยู่ในส่วนใดของผิวเซลล์
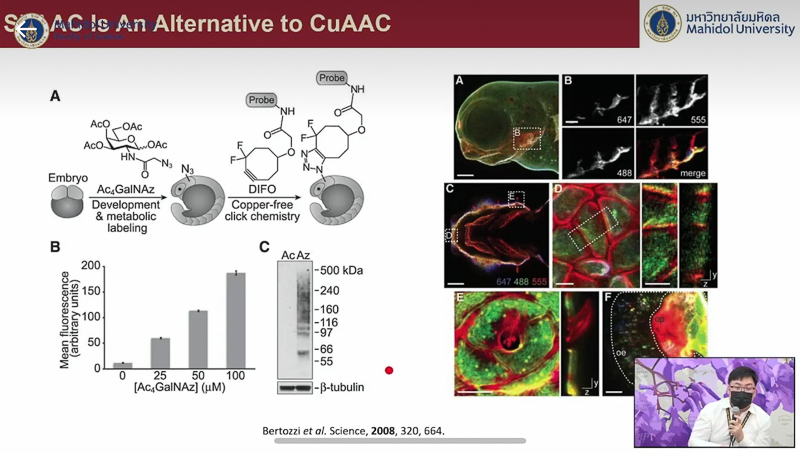
จากนั้นในปี ค.ศ. 2008 ศาสตราจารย์เบอร์ทอซซี ได้ทดลองติดตามโมเลกุลน้ำตาลในระบบของสิ่งมีชีวิตได้สำเร็จ โดยนำเอาโมเลกุลน้ำตาลที่มีความสำคัญกับการพัฒนาตัวอ่อนของปลาม้าลาย (Zebrafish) และมีหมู่ฟังก์ชันอะไซด์อยู่ ใส่ลงในอาหารเลี้ยงตัวอ่อน และเมื่อโมเลกุลน้ำตาลไปแสดงออกผิวเซลล์ซึ่งกำลังเจริญเติบโต จึงใช้ปฏิกิริยาคลิกเพื่อติดฉลากสี ทำให้สามารถติดตามตำแหน่งของโมเลกุลน้ำตาลในช่วงระยะเวลาต่าง ๆ บนตัวอ่อนได้ ซึ่งปฏิกิริยาคลิกที่ใช้นั้นมีความพิเศษตรงที่ไม่ได้ใช้ไอออนของทองแดงเป็นตัวเร่งของปฏิกิริยา เนื่องจากเป็นพิษต่อเซลล์ แต่ใช้สารตั้งต้นในการทำปฏิกิริยาที่มีพลังงานสูง ทำให้ปฏิกิริยาเกิดขึ้นได้ง่ายโดยไม่ต้องพึ่งตัวเร่งปฏิกิริยา และสามารถประยุกต์ใช้ปฏิกิริยาเคมีไบโอออร์โทโกนอลดังกล่าวในสิ่งมีชีวิตได้ในที่สุด


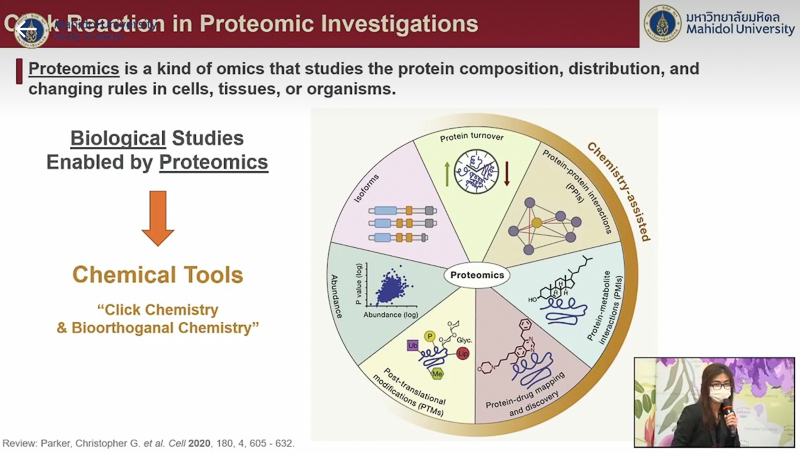
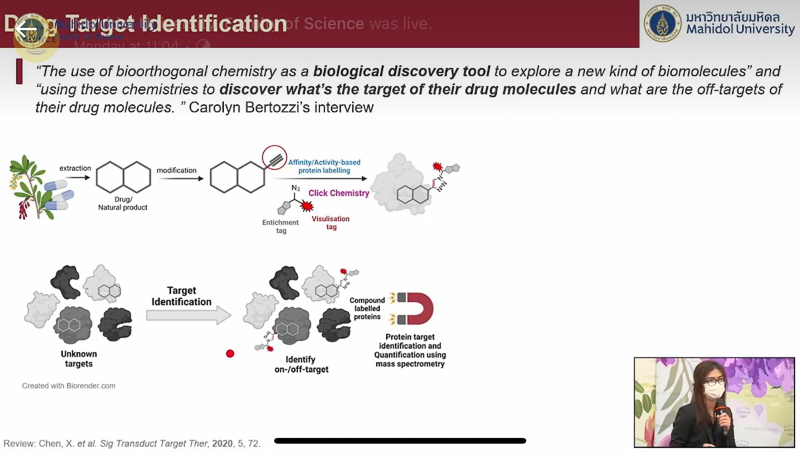
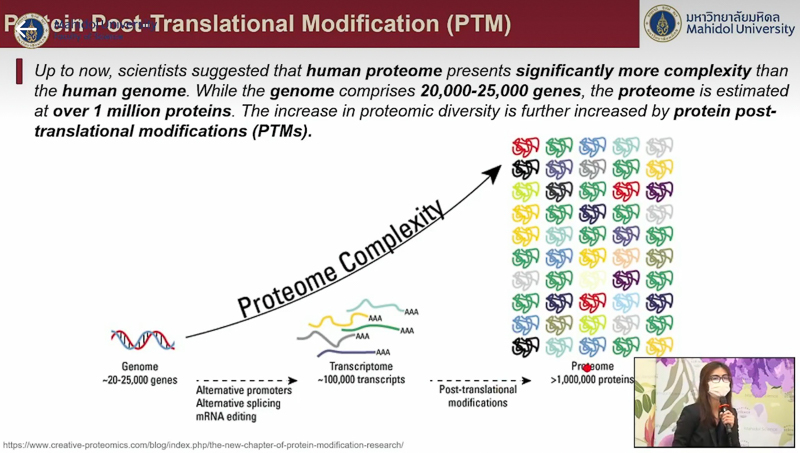
ด้าน อาจารย์ ดร.ณัฐวดี ปัญญาอินทร์ ได้กล่าวเสริมถึงการประยุกต์ใช้เคมีไบโอออร์โทโกนอลในการศึกษาด้านโปรตีโอมิกส์ (Proteomics) ซึ่งช่วยเติมเต็มการศึกษาเจาะลึกสิ่งที่เกิดขึ้นระหว่างโปรตีนกับยา โปรตีนกับสารเคมีในกระบวนการสร้างและสลายของร่างกาย และโปรตีนกับโปรตีนด้วยกันเอง โดยยกข้อความจากบทสัมภาษณ์รางวัลโนเบล ศาสตราจารย์เบอร์ทอซซี ซึ่งกล่าวว่า เคมีไบโอออร์โทโกนอลเป็นเครื่องมือสำรวจทางชีววิทยาเพื่อศึกษาโมเลกุลใหม่ มีการใช้มากในการศึกษาเป้าหมายหลักของยา และเป้าหมายนอกเหนือจากนั้น ที่อาจได้รับผลกระทบจากยาชนิดนั้นด้วยซึ่ง อาจารย์ ดร.ณัฐวดี ได้ยกตัวอย่างการหาเป้าหมายของยา เช่น ยารักษาโรคอ้วนซึ่งอาจมีประสิทธิภาพในการนำมารักษาโรคมะเร็งได้ รวมถึงสามารถใช้ศึกษาความหลากหลายของหน้าที่โปรตีนในร่างกายมนุษย์ อันเกิดจากการดัดแปลงโมเลกุลของโปรตีนหลังการถอดรหัส (Protein Post – Translational Modifications: PTMs) ซึ่งจะช่วยไขปริศนาสาเหตุความผิดปกติของโปรตีนที่เป็นตัวการให้เราป่วย และพัฒนายารักษาโรคต่าง ๆ ได้ง่ายขึ้น พร้อมนำเสนอผลงานการวิจัยที่ผ่านมา อาทิ การศึกษาเป้าหมายข้างเคียงของตัวยับยั้งโปรตีน UCHL-1 และการศึกษาตำแหน่งของโมเลกุลจากการแปลงรหัสที่ติดอยู่กับโปรตีน เป็นต้น


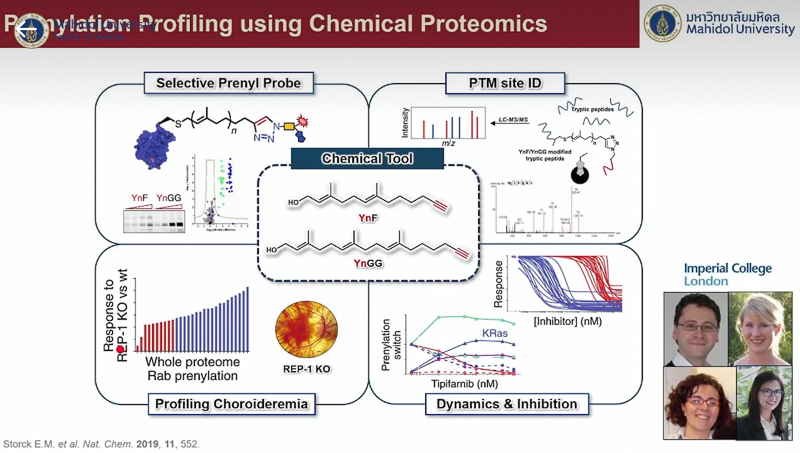
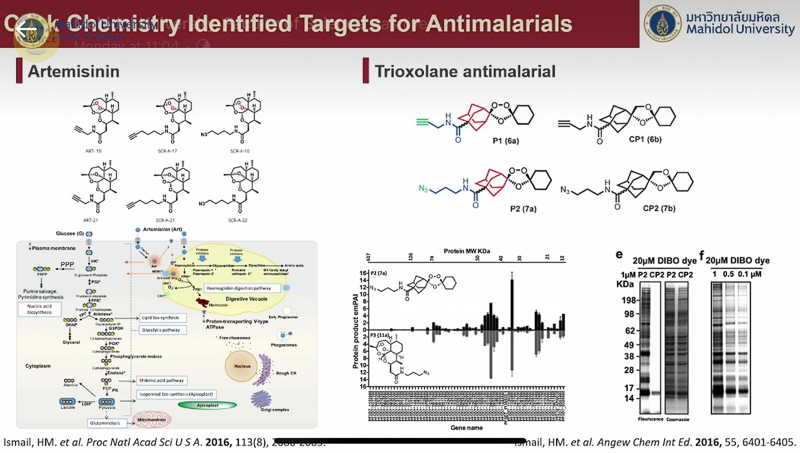
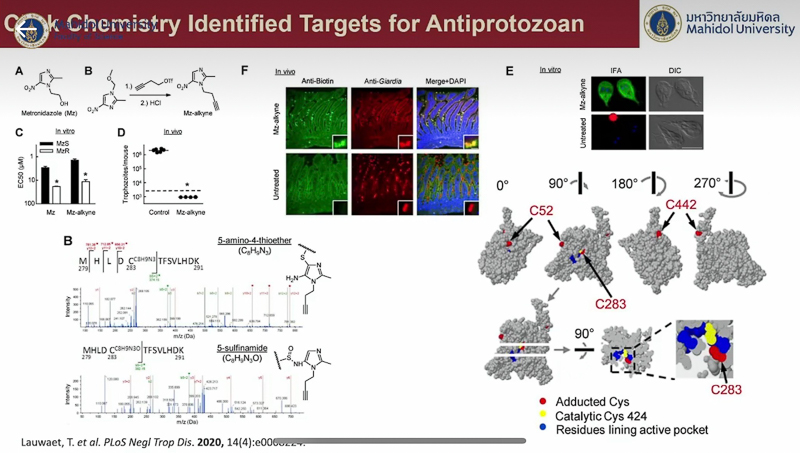
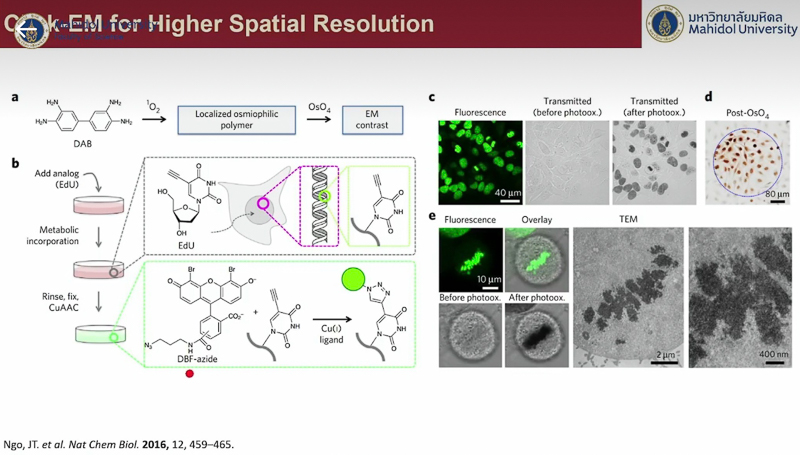
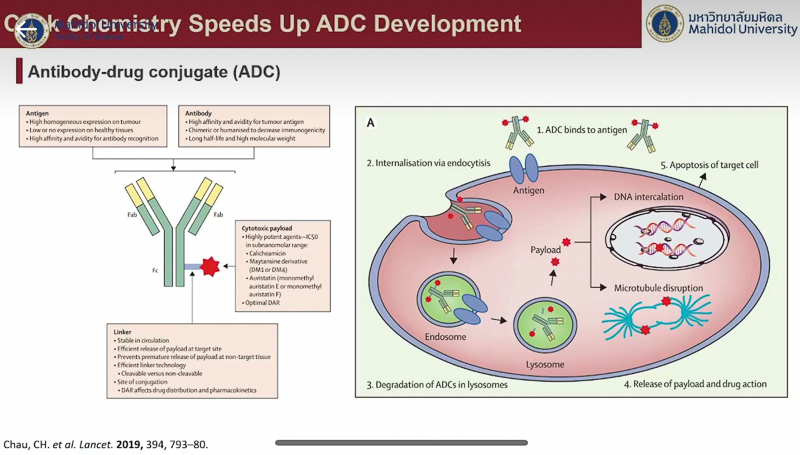
ปิดท้ายด้วย อาจารย์ ดร.มัทธิว พันชนะ ซึ่งได้ยกตัวอย่างการใช้เคมีไบโอออร์โทโกนอลในเซลล์สิ่งมีชีวิต โดยกล่าวย้อนไปถึงงานวิจัยของ ศาสตราจารย์เบอร์ทอซซี เมื่อปี ค.ศ. 2007 ซึ่งศึกษาการเปลี่ยนแปลงของน้ำตาลในเซลล์ โดยติดฉลากสีที่โมเลกุลของน้ำตาล ทำให้เห็นว่าโมเลกุลของน้ำตาลมีการเข้า-ออกเซลล์อยู่ตลอดเวลา และงานวิจัยของ ดร. ชาร์ปเลส เมื่อปี ค.ศ. 2020 ที่ศึกษาเป้าหมายของยา Metronidazoie พบว่ายาเข้าไปสู่เซลล์ของเชื้อก่อโรคได้จริง และยังระบุตำแหน่งที่ยาไปเกาะติดกับกรดอะมิโนที่มีความสำคัญต่อการเร่งปฏิกิริยาของเอนไซม์อันเป็นเหตุให้ฆ่าเชื้อได้อีกด้วย พร้อมยกตัวอย่างงานวิจัยที่ตนเองและ อาจารย์ ดร.สิทธิวุฒิ ร่วมกันศึกษาหาตำแหน่งเป้าหมายของ Artemisinin ยารักษาโรคมาลาเรียจากการคิดค้นของ ศาสตราจารย์ ถู โยวโยว (Professor Youyou Tu) เจ้าของรางวัลโนเบล สาขาสรีรวิทยาหรือการแพทย์ ปี ค.ศ. 2015 ซึ่งได้ผลในการรักษาดีมากแต่ตำแหน่งเป้าหมายโปรตีนของยายังเป็นปริศนา พบว่ายาตัวนี้มีโปรตีนเป้าหมายกว่า 100 ตัว ทำให้เกิดการยับยั้งการทำงานของเชื้อ และได้ทดสอบกับยาต้านมาลาเรียในกลุ่มเดียวกันก็พบว่ายามีโปรตีนเป้าหมายที่หลากหลายเช่นเดียวกัน นอกจากนั้นยังกล่าวถึงงานวิจัยที่ยกระดับการประยุกต์ใช้ไปอีกขั้นด้วยการติดตามตำแหน่งของโมเลกุลที่ทำปฏิกิริยาคลิกจากกล้องจุลทรรศน์อิเล็กตรอน ซึ่งช่วยให้เราเห็นภาพที่ละเอียดมากขึ้น และการพัฒนาคอนจูเกตยา-แอนติบอดี (Antibody-Drug Conjugate) ซึ่งทำให้โมเลกุลของยาเชื่อมเข้ากับแอนติบอดีได้เฉพาะเจาะจง ส่งผลให้มีประสิทธิภาพในการใช้งานมากขึ้น


ในตอนท้ายของการเสวนาวิทยากรทั้ง 4 ท่านได้กล่าวถึงผลงานวิจัยจากผู้ได้รับรางวัลโนเบล สาขาเคมี ในปีนี้ว่า “Click Chemistry” เป็นปฏิกิริยามีความเรียบง่าย และมีความจำเพาะสูงกับหมู่ฟังก์ชันเพียง 2 ชนิด ซึ่งช่วยเปิดโลกของเคมีสังเคราะห์ ทำให้เราสามารถสังเคราะห์โมเลกุลที่มีความซับซ้อนสูงและปรับแต่งคุณสมบัติของวัสดุได้ตามต้องการ และยังสามารถลดความยุ่งยากในการศึกษากลไกการทำงานในสิ่งมีชีวิต ทำให้เราศึกษาสิ่งต่าง ๆ ได้ลึกซึ้งยิ่งขึ้น แสดงให้เห็นถึงความงามของวิทยาศาสตร์ที่เริ่มต้นจากองค์ความรู้ของศาสตร์หนึ่งแต่สามารถสร้างผลกระทบในวงกว้างสู่ศาสตร์อื่น ๆ ซึ่งช่วยเปิดประตูสู่ความเป็นไปได้ใหม่ ๆ อีกมากมาย
ทั้งนี้ ผู้ที่สนใจสามารถรับชมการเสวนา Nobel Prize in Mahidol Science Cafe Vol.2: สู่ยุคของโมเลกุลเชิงหน้าที่ Click Chemistry and Bioorthogonal Chemistry: Entering the Era of Functionalism ย้อนหลังได้ที่ https://fb.watch/gv0NcAVQlA/









เขียนข่าว : นางสาวปัณณพร แซ่แพ
ตรวจสอบโดย : รองศาสตราจารย์ ดร.ปรียานุช แสงไตรรัตน์นุกูล,
อาจารย์ ดร.สิทธิวุฒิ เจริญสุทธิวรากุล,
อาจารย์ ดร.ณัฐวดี ปัญญาอินทร์,
อาจารย์ ดร.มัทธิว พันชนะ
ภาพข่าวโดย: นางสาวสุภาวดี เพ็ชร์น้อย
เว็บมาสเตอร์: นางสาวปัณณพร แซ่แพ
วันที่ 31 ตุลาคม 2565
จำนวนคนดู: 405