| เอนไซม์ลูซิเฟอเรส (Bacterial luciferase; Lux) |
เอนไซม์ลูซิเฟอเรส (bacterial
luciferase; Lux) เป็นเอนไซม์ที่ทำหน้าที่เร่งปฏิกิริยาออกซิเดชันของออกซิเจน
รีดิวซ์ฟลาวิน โมโนนิวคลีโอไทล์ (FMNH-),
และอัลดีไฮด์ (aldehyde) ทำให้ได้มาซึ่งสารผลิตภัณฑ์
คือ กรดไขมัน (fatty acid) ออกซิไดซ์ฟลาวิน
(FMN) น้ำ และเปล่งแสงสีเขียวแกมน้ำเงินออกมา
(ดังแสดงในรูป)
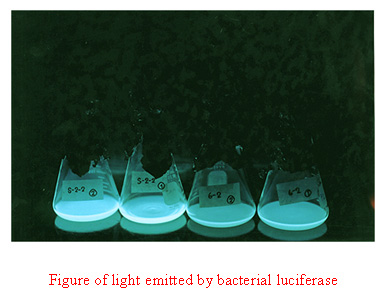
ซึ่งเอนไซม์ชนิดนี้ได้มีรายงานการค้นพบในแบคทีเรีย
3 ชนิดคือ Vibrio, Photobacterium
และ Xenorhabdus ปฏิกิริยาการเร่งของเอนไซม์ลูซิเฟอเรส
สามารถนำมาเป็นต้นแบบประยุกต์ในด้านวิทยาศาสตร์การแพทย์
เช่น เป็นตัวตรวจวัดชีวภาพเพื่อการตรวจวินิจฉัยโรค
เป็นต้น เราได้ทำการคัดแยกสายพันธุ์ของแบคทีเรียที่มีเอนไซม์
Lux โดยเก็บตัวอย่างสิ่งมีชีวิตในทะเลจากดิน
ทราย น้ำ และปลาทะเล บริเวณชายฝั่งทะเลทางตอนใต้ของประเทศไทย
ตั้งแต่จังหวัดชุมพร พังงา ภูเก็ต จนถึงตรัง
พบว่า Vibrio campbellii จากน้ำทะเลเป็นแบคทีเรียที่สามารถเรืองแสง
ซึ่งสามารถผลิตเอนไซม์ Lux ได้ และยังไม่เคยมีรายงานถึงการค้นพบดังกล่าวมาก่อน
เราจึงได้ โคลนและทำการแสดงออกของยีน
Lux จากเชื้อแบคทีเรียชนิดนี้ในแบคทีเรีย
E. coli ให้ได้ปริมาณเอนไซม์ที่มากพอเพื่อใช้
ในงานวิจัย จากการศึกษาคุณสมบัติของเอนไซม์นี้พบว่า
สามารถทนความร้อนได้ดี และสามารถเร่งปฏิกิริยาได้ดีกว่าเอนไซม์
Lux ที่เคยมีรายงานมาก่อน (J. Biochem.
(Tokyo) 142(4), 539-552)
ดังที่กล่าวข้างต้น เอนไซม์
Lux ใช้รีดิวซ์ฟลาวิน (FMNH-) เป็นสารตั้งต้นซึ่งสารนี้เป็นสารที่ไม่เสถียร
สามารถเกิดปฏิกิริยากับ ออกซิเจนได้ง่าย
ดังนั้นในเซลล์จึงจำเป็นจะต้องมีเอนไซม์รีดักเทส
เพื่อทำหน้าที่เร่งปฏิกิริยาการรับอิเล็กตรอนจาก
NADH
ให้ได้รีดิวซ์ฟลาวิน เพื่อส่งถ่ายให้กับเอนไซม์
Lux จากการศึกษาก่อนหน้านี้พบว่าบน
Lux operon ประกอบด้วยยีนที่ทำหน้าที่ในการผลิตเอนไซม์
ที่ทำให้เกิดปฏิกิริยาการเรืองแสง และ
LuxG เป็นยีนที่คาดว่าน่าจะทำหน้าที่ในการผลิตเอนไซม์รีดักเทสดังกล่าว
แต่ยังไม่เคยมีรายงานการวิจัยเรื่องนี้มาก่อน
ดังนั้นเราจึงทำการคัดแยกโปรตีน LuxG
จากแบคทีเรีย Photobacterium
leonathi TH1 ซึ่งเราเป็นกลุ่มแรกที่โคลน
และทำการแสดงออกของยีน LuxG ในแบคทีเรีย
E. coli ซึ่งสามารถผลิตโปรตีน
LuxG และ LuxG ที่มีกรดอะมิโนฮิสทิดีน
ติดอยู่ที่ปลาย C-terminus ซึ่งโปรตีนทั้งสองรูปแบบ
สามารถทำให้บริสุทธิ์ได้โดยการ ใช้เทคนิคทางโครมาโตกราฟี
จากการศึกษาคุณลักษณะของโปรตีน LuxG
พบว่า สามารถทำหน้าที่เป็นเอนไซม์ฟลาวินรีดักเทส
(flavin reductase) ที่ทำหน้าที่เร่งปฏิกิริยารีดักชันของฟลาวิน
(FMN, FAD และ riboflavin) โดยใช้อิเล็กตรอนจาก
NADH นอกจากนี้ จากการศึกษาการทำงานร่วมกันในหลอดทดลอง
ของเอนไซม์ Lux และเอนไซม์ LuxG พบว่า
LuxG สามารถที่จะผลิต FMNH- ที่เป็นสารตั้งต้นให้กับเอนไซม์
Lux ได้ และจากการศึกษาการควบคุมยีน
ไม่ให้ผลิตโปรตีน LuxG (LuxG-knockout)
ผลปรากฎว่าทำให้แบคทีเรียไม่เกิดปฏิริยาเรืองแสงได้
จากการศึกษาจลนพลศาสตร์ของเอนไซม์ LuxG
ทำให้เราทราบว่ากลไกการเกิดปฏิกิริยาเป็นแบบ
ternary complex (J. Bacteriology
(2008), 1531-1538)

เป้าหมายของงานวิจัย
1. เพื่อศึกษากลไกการเร่งปฏิกิริยาของเอนไซม์
LuxG และกลไกการส่งถ่ายรีดิวซ์ฟลาวิน
(FMNH-) จากเอนไซม์ LuxG
ไปยังเอนไซม์ Lux
2. เพื่อประยุกต์เอนไซม์ลูซิเฟอเรสเป็นตัวตรวจวัดชีวภาพ
(biosensor) เพื่อใช้ในการตรวจวินิจฉัยโรค
ติดต่อเรา:
ห้องปฏิบัติการ (LAB) PR305 ตึก PR
ชั้น 3
ภาควิชาชีวเคมี
คณะวิทยาศาสตร์ มหาวิทยาลัยมหิดล
ถนนพระรามที่ 6 กรุงเทพฯ 10400
โทร. 02-201-5596
หน่วยวิจัยโครงสร้างและการทำงานของโปรตีน
(CPSF)
อาคารเฉลิมพระเกียรติ ชั้น 4 ห้อง K419
คณะวิทยาศาสตร์ มหาวิทยาลัยมหิดล
272 ถนนพระรามที่ 6 กรุงเทพฯ 10400
โทร: 02-201-5847 โทรสาร : 02-201-5843
e-mail : pimchai.cha@mahidol.ac.th
|